Place de l’électrothérapie pour les patients Covid-19 sévères pendant la phase post-réanimation

Partout en France, des patients Covid-19 sont pris progressivement en charge pour des soins de suite et de réadaptation après un long séjour en réanimation. Comment tâcher de prévenir les complications liées à la réanimation ? Quelle rééducation proposée pour les patients Covid + après une hospitalisation souvent très lourde ? De quels soins ont-ils besoin lors de leur retour à domicile ?
Prise en charge des patients Covid+ après réanimation
Orientation des patients
En sortie de réanimation ou de soins continus en infectiologie, les patients sont pour la plupart orientés vers des unités de Médecine Physique et de Réadaptation (MPR). Egalement vers de Soins de suite et de réadaptation (SSR) spécialisées dans les affections respiratoires. Les patients les plus graves sont reçus dans des Services de Rééducation Post Réanimation (SRPR) dédiés. Ils créés en liens étroits avec des réanimateurs et des pneumologues.
Dans ces unités, les patients souvent extrêmement affaiblis suivent un programme individualisé. Et le chemin s'annonce très long car les séquelles possibles sont liées aux atteintes de l'infection virale et à l’orage hyper-inflammatoire du système immunitaire. D'autres sont liées :
- aux complications du syndrome de détresse respiratoire aiguë (SDRA),
- aux séquelles neurologiques,
- à l'immobilité
- au séjour prolongé en soins intensifs
Publication de la HAS
Pour répondre aux questions sur cette prise en charge SSR très particulière et le retour à domicile, la Haute autorité de Santé (HAS) vient de publier un premier document avec la participation de différentes sociétés savantes, dont la SOFMER (Société Française de Médecine Physique et de Réadaptation).
Dans cette publication, la HAS insiste sur le fait que « la rééducation s'apparente à celle d'un Syndrome de Détresse Respiratoire Aiguë (SDRA) pour les patients ayant séjourné en réanimation, et à celle d’un patient déconditionné pour les patients les moins sévères, avec deux particularités :
- la forte contagiosité de l'infection virale qui nécessite de maintenir les mesures de protection jusqu'à une décision pluridisciplinaire de levée d'isolement intégrant des infectiologues ;
- la fragilité de ces patients susceptibles de présenter des décompensations médicales brutales à type de défaillance respiratoire, de complications thrombo-emboliques ou cardiovasculaires. »
Complications possibles
La réanimation est également pourvoyeuse de complications, d'autant que certains patients restent intubés et ventilés plus de dix jours. Certains ont été mis en position de décubitus ventral 16h par jour ce qui est très éprouvant pour le corps.
Les déficiences recensées sont :
- neuromyopathies acquises liées à l'utilisation de certains médicaments et aggravées par l'absence de mobilisation musculaire ;
- troubles de la déglutition ;
- complications métaboliques majeures avec des pertes de poids très importantes en peu de temps ;
- complications orthopédiques.
De tout ceci, découle un grand déconditionnement cardiorespiratoire et musculaire à l'effort indique le rapport HAS.
Intérêt de l’électrostimulation pour les patients en réanimation
L’étude de Roeseler[1] publiée en 2013 constate que « les données sur les effets de l’électrostimulation en réanimation montrent une augmentation de la force musculaire[2-4] , une diminution de l’atrophie du ou (des) groupe(s) musculaire(s) stimulé(s)[5,6] et une augmentation de la distance de marche[2].
L’électrostimulation limite le catabolisme musculaire des patients immobilisés en réanimation[7]. Plusieurs sessions quotidiennes d’électrostimulation semblent préserver la masse musculaire (évaluée par échographie) et avoir des effets positifs sur la micro-circulation des tissus musculaires[6][8], etc. que les patients traités par électrostimulation présentent un score mRc (medical Research council)[9] plus élevé, sont sevrés plus rapidement de la ventilation mécanique et développent moins de polyneuromyopathies[10]. De plus, cette technique ne semble pas avoir d’incidence sur les fréquences cardiaque et respiratoire, la saturation en o2 et la pression artérielle[6]. Elle peut donc être instaurée précocement. L’électrostimulation peut être proposée à des patients conscients [2] ou inconscients[6] en réanimation. »
Intérêt de l’électrostimulation neuromusculaire pour les patients atteints de syndrome de déconditionnement SDRA*
Explication
Le terme "Déconditionnement à l’effort" peut s’appliquer pour de nombreuses situations. Il en résulte une restriction plus ou moins sévère, mais toujours prolongée de l’activité physique.
Les sérieuses altérations musculaires mises en évidence chez les patients souffrant d’une insuffisance respiratoire chronique sont dues :
- en partie à la sédentarité et/ou à l’insuffisance fonctionnelle imposée par la mauvaise adaptation à l’effort
- à une véritable myopathie, c’est-à-dire à une atteinte structurelle des fibres musculaires qui ne résulte pas de ce déficit d’utilisation
Le capital musculaire du patient BPCO est aujourd’hui considéré comme son "baromètre de vie". Avec un pronostic vital à cinq ans, étroitement corrélés à ses capacités musculaires périphériques, quelques chiffres parlent d’eux-mêmes :
Les quadriceps de patients BPCO stables présentent en moyenne une diminution de leur endurance de 50%. Ils présentent aussi un déficit de force de 30%. Cela conduit inéluctablement à une réduction de la capacité des patients à pouvoir accomplir les gestes de la vie quotidienne.
Cause de myopathie
Parmi les causes identifiées de cette myopathie figurent :
- les pics inflammatoires,
- le stress oxydant,
- les médications utilisées (corticoïdes+++)
- le déséquilibre nutritionnel
C’est surtout lors des phases de décompensation que ces différentes conditions atteignent leur paroxysme, ce qui explique la perte de force de 20% qui apparaît dès le 3ème jour d’une phase d’exacerbation. En l’absence d’une prise en charge musculaire spécifique, la récupération est quasi nulle puisque la force du quadriceps n’est augmentée que de 6%, trois mois après la phase de décompensation.
[caption id="attachment_229" align="aligncenter" width="188"] Amyotrophie du quadriceps – patient BPCO[/caption]
Amyotrophie du quadriceps – patient BPCO[/caption]
Role de l'électrostimulation
C’est dans ce contexte que l’électrostimulation s’inscrit comme une technique de choix en permettant d’imposer une activation musculaire à la fois qualitative en adoptant un régime de travail adapté à la physiopathologie des muscles stimulés, mais aussi quantitative en évitant la sollicitation cardio-vasculaire et la dyspnée, tout en étant aujourd’hui une technique confortable à défaut d’être agréable.
Sur le plan fonctionnel, un parallèle peut être fait entre l’insuffisant respiratoire (BPCO) et l’attaque virale liée au Covid-19. Nous sommes face à une altération généralisée de l’organisme avec un alitement prolongé engendrant une atrophie musculaire. Dès que possible et sur avis médical seulement, on pourra envisager une rééducation à visée locomotrice où l’électrostimulation s’intégrera parfaitement.
Le programme de rééducation exposé ci-après se fera en respectant les règles d’hygiènes sanitaires obligatoires pour assurer la protection du thérapeute. Il s’associera à l’ensemble des techniques mis en place sur le plan respiratoire ainsi qu’aux mobilisations articulaires passives et/ou actives.
Electrothérapie
Protocole
Le renforcement musculaire des membres inférieurs sera donc l’objectif principal du protocole. En effet, la priorité est donnée à la récupération de l’autonomie de marche.
La stimulation des quadriceps se fait au moyen de programmes proposés dans les appareils Chattanooga- Gamme professionnelle (Rehab/Theta/Physio/Wireless Professional) couramment utilisés pour le traitement de l’amyotrophie (Programme 35 – 45 Hz).
Objectif
Le but au départ sera d’accoutumer le patient à la stimulation. Il n’est donc pas nécessaire d’augmenter fortement les intensités ni de faire la totalité du programme mais d’assurer plutôt un suivi réactionnel du patient.
Cette stimulation pourra être quotidienne si bien supportée. L’intérêt d’un appareil sans fil type Wireless Professional assurera une distance de sécurité avec le patient tout en veillant à respecter les mesures de décontamination des modules dans le cadre d’une contagiosité potentielle liée à l’infection virale.
Séances
Il est fondamental de commencer par le programme amyotrophie niveau 1 dont les paramètres sont présentés ci-dessous. Vous devez vous adapter bien entendu au cas clinique mais en général, il est toujours intéressant de faire environ 5 à 6 séances sur ce niveau. Objectif : levée de sidération si besoin, découverte du rythme contraction/repos, début de trophicité musculaire.
Dans les semaines qui suivent l’utilisation du niveau 2 (voir paramètres) à raison de 3 séances minimum par semaine accompagnera les séances de rééducation musculaire et proprioceptive. Son objectif : redonner une bonne trophicité, du volume et de la force musculaire. Il sera possible d’envisager un travail volontaire associé dès que l’état de santé du patient le permettra.
[caption id="attachment_233" align="aligncenter" width="655"]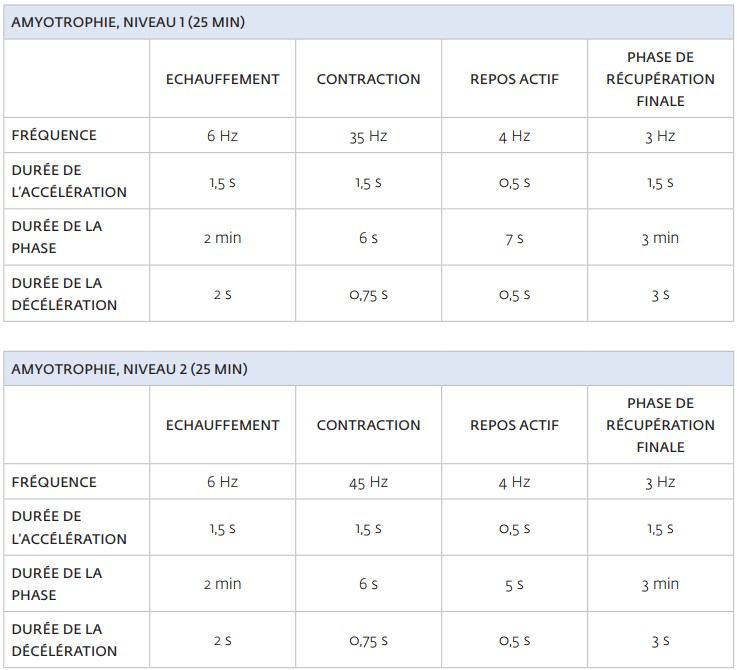 Paramètres de stimulation[/caption]
Paramètres de stimulation[/caption]
Exemples
Voici présentés deux exemples de position de travail. On n’oubliera pas de sangler les extrémités des membres inférieurs. Cela permet d’éviter l’extension du genou qui pourrait rendre la contraction électro-induite douloureuse. En position couchée, un coussin sous les genoux sera placé pour maintenir une position angulaire d’environ 30°.
Rappel : Ne pas oublier que l’électrostimulation peut être pratiquée debout sous forme de petits squats. Dans ce cas, faire des répétitions de 10 exercices maximum en suivant le rythme imposé par l’appareil. Ces exercices seront faits en fin de rééducation en vue du ré-entrainement à l’effort et fonction de l’état de santé du patient. L’usage d’électrodes individuelles est vivement recommandé en particulier dans le contexte sanitaire actuel.
[caption id="attachment_232" align="aligncenter" width="565"]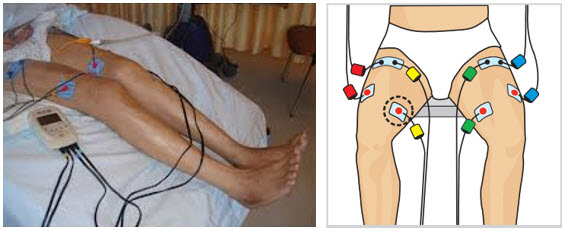 Positionnement des électrodes[/caption]
Positionnement des électrodes[/caption]
Bénefices
Les gains obtenus à la suite d’un entraînement de quatre à six semaines par électrostimulation sont extrêmement prometteurs:
| au niveau segmentaire | La force et l’endurance progressent d’au moins 35% |
| au niveau fonctionnel | Les tests de terrain ou de laboratoire utilisés montrent tous une amélioration significative de la tolérance à l’effort des patients ayant bénéficié de la stimulation comparativement aux patients des groupes témoins. |
Ces bénéfices majeurs restent surtout associés à l’amélioration de la qualité de vie objectivée par différents questionnaires (MCQ, MRF-28…) [11].
CONCLUSION
L’électrostimulation neuromusculaire se présente donc comme une technique remarquable pour les patients Covid+ les plus sévères en période de réanimation. Mais aussi lors de la prise en charge rééducative afin de prévenir puis restaurer leur potentiel musculaire à un niveau suffisant. Cela permettra d'aborder des exercices de réadaptation plus globaux à moyen terme. Cette méthode devra être poursuivie lors du retour à domicile et sera favorisée par l’apport des technologies d’électrothérapie portable.
La douleur est un signe qu’il ne faut pas négliger. Si cette dernière est prononcée et/ou perdure trop longtemps, il est conseillé de consulter un médecin.
Pour plus d’informations sur les solutions thérapeutiques proposées, cliquez ICI.
Auteur : Thierry SERENARI, Kinésithérapeute du Sport (Versailles) - Kiné référent de la FFE.
Consultant Chattanooga/DJO pour l’Electrothérapie.
* type Bronchopathie Chronique Obstructive BPCO
Bibliographie
(1) Roeseler J, Sottiaux T, Titomanlio L. Prise en charge de la mobilisation précoce en réanimation, chez l’adulte et l’enfant (électrostimulation incluse). Réanimation 2013;22(2):207-8.
(2) Abdellaoui a, Prefaut c, Gouzi F, et al (2011). skeletal muscle effects of electrostimulation after coPd exacerbation: a pilot study. eur Respir J 38:781–8 47.
(3) Vivodtzev i, Pepin JL, Vottero G, et al (2006). improvement in quadriceps strength and dyspnea in daily tasks after 1 month of electrical stimulation in severely deconditioned and malnourished coPd. chest 129:1540–8 48.
(4) Zanotti e, Felicetti G, maini m, Fracchia c (2003). Peripheral muscle strength training in bed-bound patients with coPd receiving mechanical ventilation: effect of electrical stimulation. chest 124:292–6 49.
(5) Gerovasili V, tripodaki e, Karatzanos e, et al (2009). short-term systemic effect of electrical muscle stimulation in critically ill patients. chest 136:1249–56 50.
(6) Meesen RL, dendale P, cuypers K, et al (2010). neuromuscular electrical stimulation as a possible means to prevent muscle tissue wasting in artificially ventilated and sedated patients in the intensive care unit: a pilot study. neuromodulation 13:315–20; discussion 321 51.
(7) Bouletreau P, Patricot mc, saudin F, et al (1987). effects of intermittent electrical stimulations on muscle catabolism in intensive care patients. JPen J Parenter enteral nutr 11:552–5 52.
(8) Gerovasili V, stefanidis K, Vitzilaios K, et al (2009). electrical muscle stimulation preserves the muscle mass of critically ill patients: a randomized study. crit care 13:R161
(9) Kleyweg RP, van der meche FG, schmitz Pi (1991). interobserver agreement in the assessment of muscle strength and functional abilities in Guillain-Barre syndrome. muscle nerve 14:1103–9 54.
(10) Routsi c, Gerovasili V, Vasileiadis i, et al (2010). electrical muscle stimulation prevents critical illness polyneuromyopathy: a randomized parallel intervention trial. crit care 14:R74
(11) Couillard A, Préfaut C. L’électrostimulation dans la réhabilitation des patients BPCO sévères : pertinence ou facétie ? Revue des maladies respiratoires. 2010; 27, 113-124
